3. Reazione di ossidazione: formazione di aldeidi, chetoni, acidi carbossilici
L’ossidazione degli alcoli dipende:
a. dalla classe di appartenenza degli alcoli
b. dalla forza dell’ossidante
Dagli alcoli primari si ottengono le aldeidi, che poi possono essere ossidate ulteriormente ad acidi carbossilici.
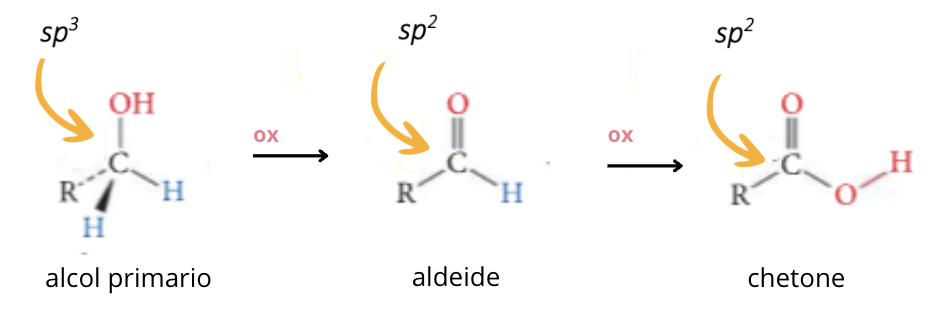
Quando un alcol si ossida ad aldeide o chetone e poi ad acido carbossilico, il numero di legami con l’ossigeno dell’atomo di carbonio aumenta da uno a due a tre, praticamente il numero di ossidazione del carbonio aumenta passando da alcol (-1) ad aldeide (+1) e infine ad acido (+3) e diminuisce il numero di atomi di idrogeno.
Gli ossidanti usati per portare gli alcoli ad acidi carbossilici sono il permanganato di potassio in ambiente acquoso (KMnO4), il bicromato di potassio in acido solforico (K2Cr2O7 ,H2SO4), si usa anche il reattivo di Jones, reagente utilizzato in laboratorio, che è anidride cromica disciolta in acido solforico acquoso (CrO3, H2SO4).
Alcuni esempi di reazioni sono i seguenti:
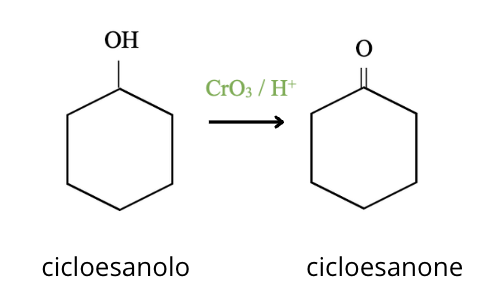
In laboratorio, il metodo migliore per fermare la reazione allo stato di aldeide è quello di usare un reagente specifico, il clorocromato di piridinio (PCC):
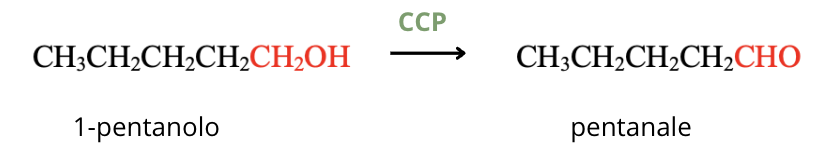
Gli alcoli secondari sono ossidati a chetoni:
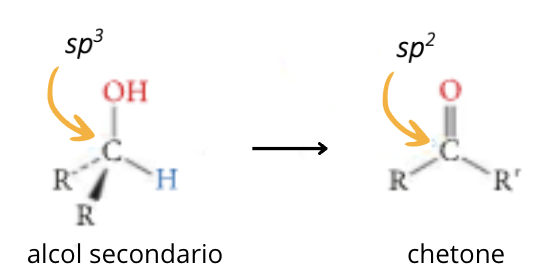
Ad esempio il 2-butanolo in presenza di un forte ossidante il permanganato di potassio in ambiente acido forma il butanone:
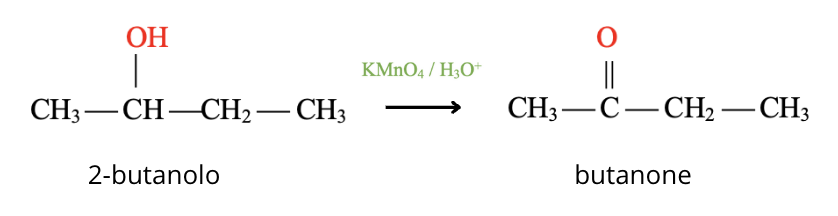
Gli alcoli terziari non avendo atomi di idrogeno sul carbonio che porta l’ossidrile, non danno reazioni di ossidazione.