2. Rottura del legame C – O; Comportamento basico
Gli alcoli comportandosi da base, accettano uno ione idrogeno da un acido. Per rompere il legame C – O è necessario un acido molto forte (acido solforico) alla temperatura di 180°C. Le reazioni di rottura del legame C – O sono:
2.1. reazione di disidratazione; il prodotto che si forma è un alchene.
2.2. reazione di idroalogenazione: il prodotto che si forma è un alogenuro alchilico
2.1. Reazione di disidratazione: formazione di alcheni
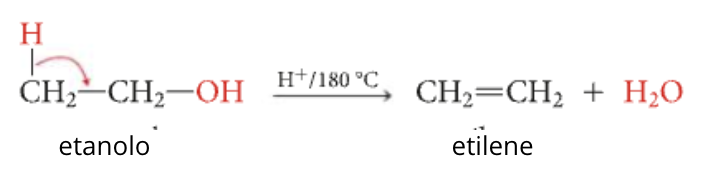
La reazione di disidratazione dell’etanolo (alcol primario) è rappresentato dalla seguente equazione:
L’alcol comportandosi da base con i suoi doppietti elettronici sull’ossigeno, attaccacono lo ione H+ l’acqua viene prima protonata e poi eliminata formando un carbocatione:
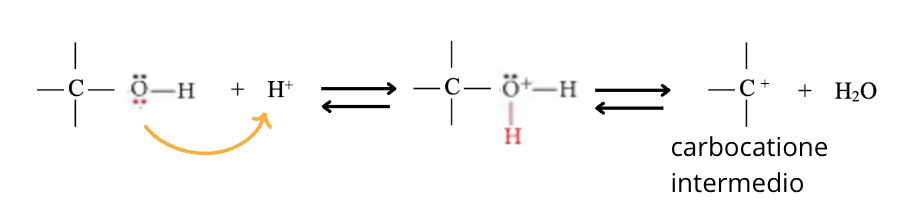
Tanto più stabile è il carbocatione intermedio, tanto più facilmente si rompe il legame C – O. Di conseguenza sono più basici gli alcoli terziari; l’ordine di basicità è il seguente:
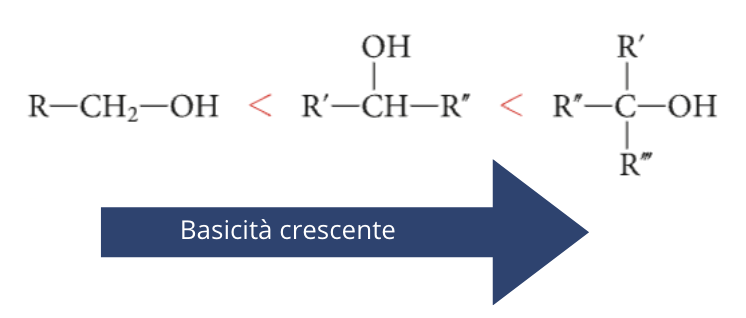
La reazione di disidratazione degli alcoli può essere impiegata come metodo di sintesi degli alcheni; è una reazione di eliminazione, che può avvenire con meccanismo E1 o E2, a seconda della classe a cui appartiene l’alcol. La disidratazione di un alcol terziario avviene con meccanismo E1, quella di un alcol primario con meccanismo E2.
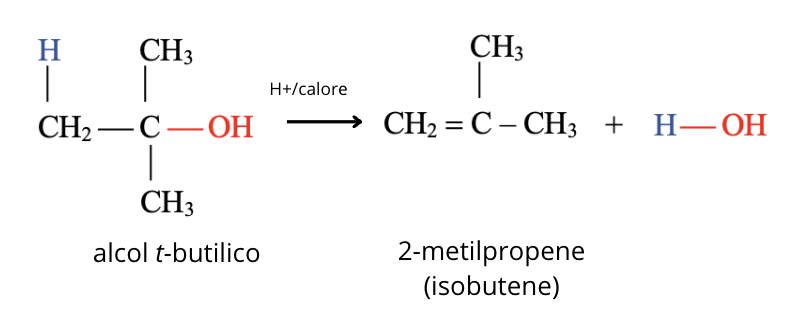
Facciamo un esempio di una reazione di disidratazione con meccanismo E1 di alcol terziario. Consideriamo l’alcol t-butilico.
Il primo passaggio comporta la protonazione reversibile del gruppo ossidrilico e la formazione di una molecola di acqua protonata:
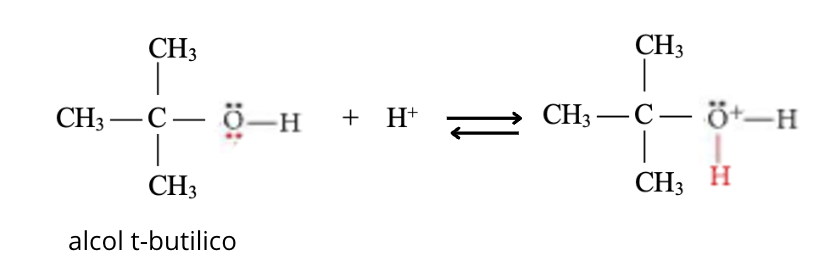
Il secondo passaggio, che è lo stadio che determina la velocità, comporta l’eliminazione dell’acqua come gruppo uscente e formazione di un carbocatione terziario:
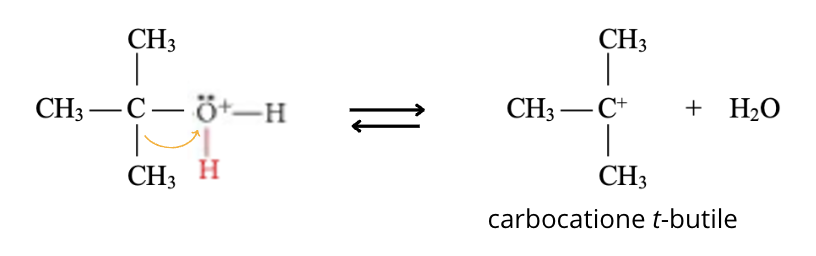
Il terzo e ultimo passaggio si completa con la perdita di un protone da un atomo di carbonio adiacente al carbocatione e formazione dell’alchene.
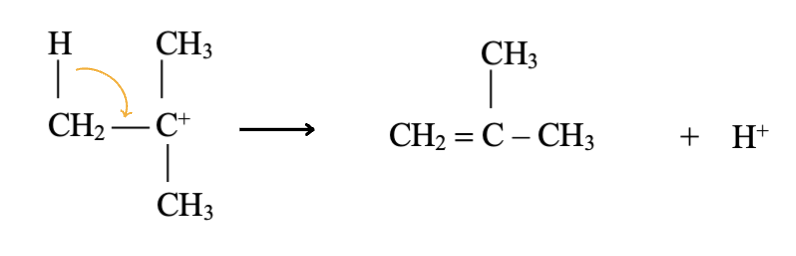
La reazione complessiva di disidratazione è data dalla somma dei tre passaggi:
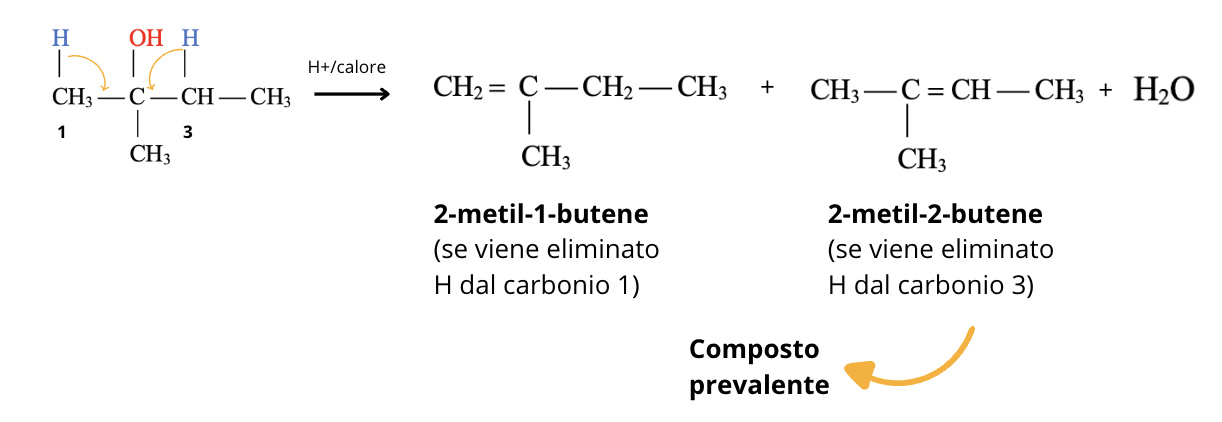
Gli alcoli secondari e terziari con almeno 4 atomi di carbonio possono dare due alcheni: l’atomo di idrogeno che viene eliminato si può staccare da uno dei due atomi di carbonio legati al carbonio del gruppo ossidrile – OH. Ad esempio dal 2-metil-2-butanolo si possono formare due alcheni. Il 2-metil-1-butene se viene eliminato l’idrogeno dal carbonio 1, il 2-metil-2-butene se viene eliminato l’idrogeno dal carbonio 3. Secondo la regola di Zaitsev prevale l’alchene con il doppio legame più sostituito, cioè con il maggior numero di gruppi alchilici legati ai carboni del doppio legame. Nel nostro esempio l’alchene prevalente è il 2-metil-2-butene.
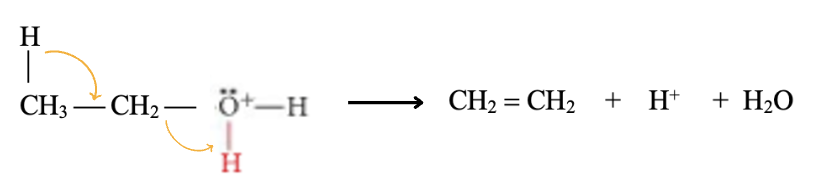
Il meccanismo della reazione di disidratazione negli alcol primari avviene senza la formazione del carbocatione primario in quanto intermedio roppo instabile; la perdita di acqua e del protone adiacente avvengono simultaneamente con meccanismo E2. Il meccanismo dell’etanolo è il seguente:
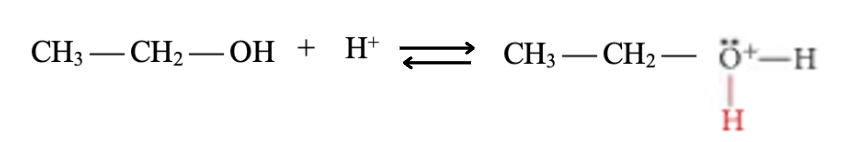
2.2. Reazione di idroalogenazione: formazione di acidi alogenidrici
Gli alcoli reagiscono con gli acidi alogenidrici (HCl, HBr, HI) per formare alogenuri alchilici (cloruri, bromuri e ioduri). In termini generali la reazione può essere così descritta:
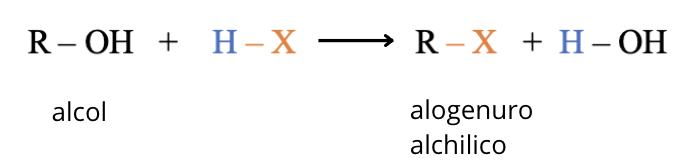
Questa reazione è di sostituzione nucleofila con meccanismo SN1 se avviene con alcol terziari. La velocità e meccanismo di reazione dipendono dalla classe di appartenenza dell’alcol, se terziario, secondario o primario, in quanto si forma un carbocatione come intermedio.
Consideriamo un alcol terziario: alcol t-butilico; la reazione procede con meccanismo SN1, attraverso un carbocatione intermedio:
Il primo passaggio comporta la protonazione reversibile del gruppo ossidrilico e la formazione di una molecola di acqua protonata:
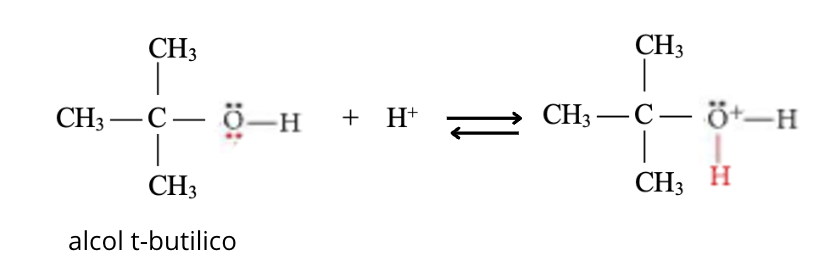
Il secondo passaggio, che è lo stadio che determina la velocità, comporta l’eliminazione dell’acqua come gruppo uscente e formazione di un carbocatione terziario:

Il terzo passaggio è l’attacco del nucleofilo lo ione cloruro al carbocatione; quest’ultimo stadio è veloce.
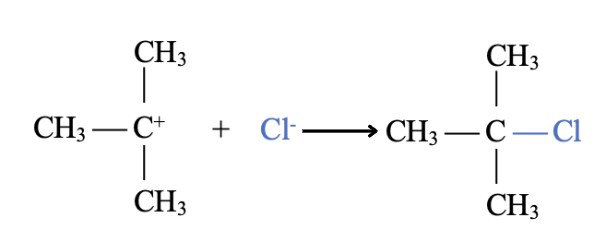
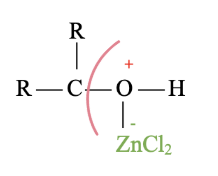
Consideriamo un alcol secondario: la reazione con velocità intermedia e con entrambi i meccanismi SN1 e SN2. La reazione essendo più lenta è catalizzata dal cloruro di zinco (acido di Lewis) che si coordina al doppietto dell’ossigeno, facilitando la rottura del legame C – O
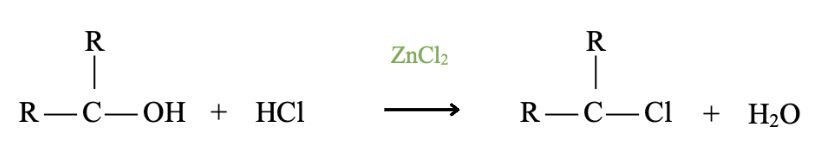
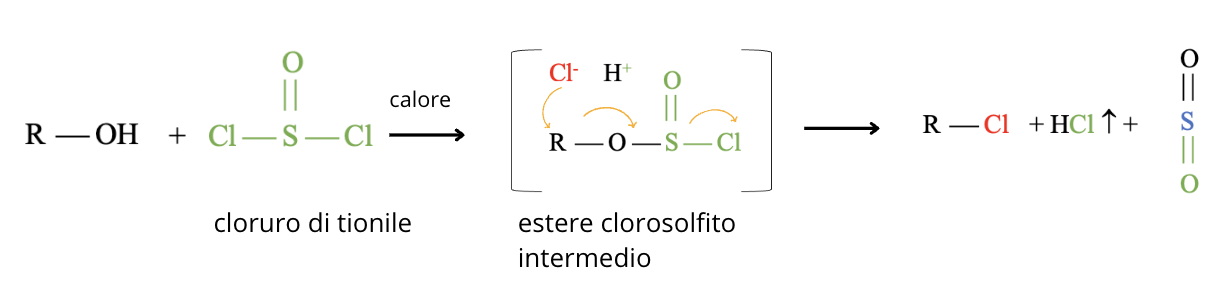
Gli alcoli primari e secondari possono essere trasformati in alogenuri alchilici per reazione con il cloruro di tionile. Si forma un estere clorosolfito che è un intermedio, seguita dalla reazione di sostituzione nucleofila SN1 o SN2, a seconda della classe di appartenenza dell’alcol.
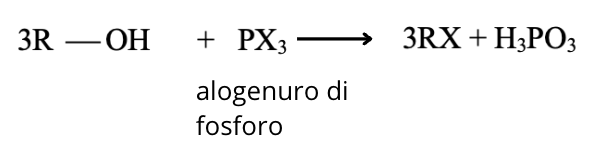
Anche gli alogenuri di fosforo, come il tribromuro di fosforo, trasformano gli alcoli in algenuri alchilici