Gli alcoli possono dare origine a tre tipi di reazioni:
1. Rottura del legame O – H (comportamento acido)
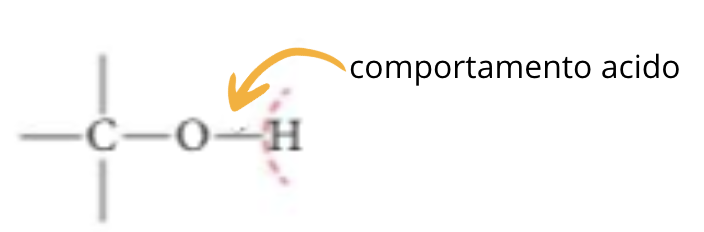
2. Rottura del legame C – O (comportamento basico)

3. Ossidazioni
1. Rottura del legame O – H; Comportamento acido
Abbiamo già visto che gli alcoli sono acidi debolissimi. La forza acida è simile al quella dell’acqua (Ka = 10–16 )
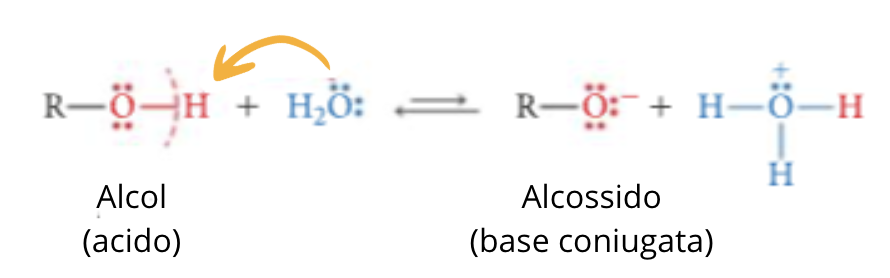
Ricordiamo anche che l’acidità aumenta passando da alcoli terziari a primari. Infatti un acido è tanto più forte quanto più è stabilizzata la sua base coniugata, a causa dell’effetto induttivo +I. Infatti, le basi coniugate degli alcoli sono tanto più stabilizzate quanto minore è il numero dei gruppi R; da ciò deriva che le più stabili sono quindi le basi derivate dell’alcol metilico e degli alcoli primari. Inotre, si deve aggiungere che l’alcossido derivante dall’alcol primario è più stabilizzato dalla solvatazione rispetto ai derivati degli alcoli secondari e teriziari, in quanto in questi l’impedimento sterico dei gruppi R ostacola l’avvicinamento dell’acqua.
L’ordine di basicità degli alcossidi è il seguente:
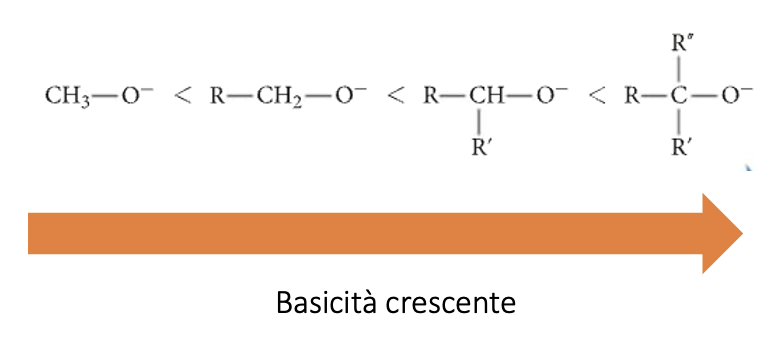
Essendo gli alcoli acidi molto deboli, la loro dissociazione ionica può avvenire solo con ambienti forti. E’ possibile rompere il legame O – H degli alcoli mediante una reazione di ossidoriduzione con metalli alcalini (simbolo Me): il metallo si ossida, mentre l’idrogeno liberato dall’alcol si riduce a idrogeno molecolare formando un sale detto alcossido o alcolati
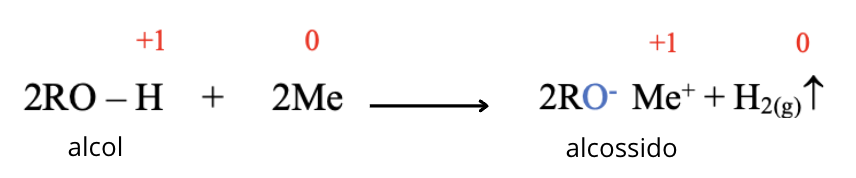
Il nome dell’alcossido è costituito dalla radice del nome dell’alcol corrispondente seguito dal suffisso -ossido, dalla preposizione di e dal nome del metallo.
La reazione tra l’etanolo e il sodio metallico è rappresentata dalla seguente equazione:
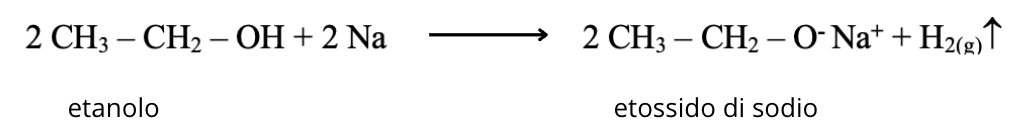
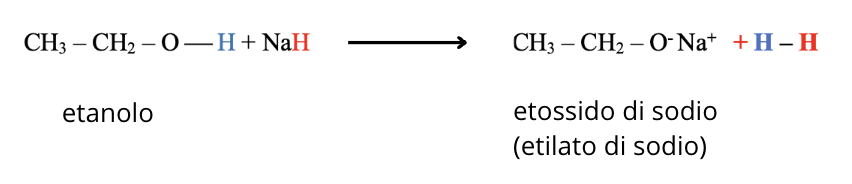
La reazione può avvenire anche con sodioammide (Idrossido di sodio non ha forza basica a sufficienza):
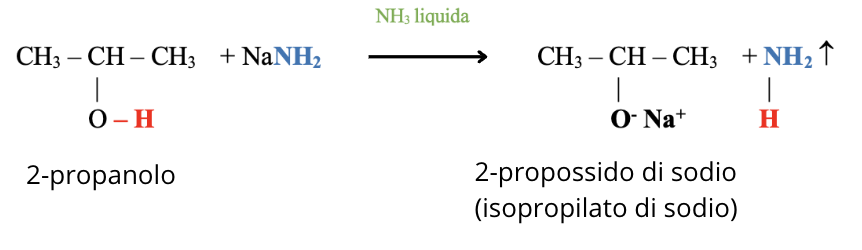
La reazione può avvenire anche con un idruro metallico: